L'attività dei sistemi enzimatici coinvolti nel metabolismo dei farmaci è sensibile agli inibitori e agli induttori enzimatici.
Un inibitore enzimatico provoca un accumulo di un altro farmaco/sostanza inibendone il metabolismo. Gli effetti clinici degli inibitori enzimatici di solito si verificano in circa 2-3 giorni, poiché il meccanismo più comune è la competizione per l'enzima che viene inibito.
Un induttore enzimatico accelera il metabolismo di un altro farmaco/sostanza. Gli effetti clinici degli induttori enzimatici richiedono più tempo rispetto agli inibitori, circa 2-3 settimane, perché il meccanismo di induzione comporta un aumento della sintesi enzimatica o un rallentamento della degradazione dell'enzima interessato.
Dei circa 4800 composti che si ritiene siano presenti nel fumo di tabacco, la maggior parte si trova nella fase del particolato. La nicotina, una sostanza naturale presente nelle foglie di tabacco, è il componente principale.
Gli idrocarburi policiclici aromatici (IPA), prodotti della combustione incompleta, sono alcuni dei principali cancerogeni polmonari del fumo di tabacco e sono anche potenti induttori di diversi isoenzimi del citocromo P450.
Gli isoenzimi più importanti indotti dal fumo sono CYP1A2 e CYP2B6. Gli IPA possono indurre anche la via metabolica della glucuronidazione.
Molti farmaci sono substrati del CYP1A2. Nei fumatori il loro metabolismo viene indotto con conseguente diminuzione clinicamente significativa degli effetti farmacologici.
In generale, in caso di sospensione del fumo, si consiglia una riduzione del 10% della dose giornaliera per i substrati CYP1A2, soprattutto per i farmaci con finestra terapeutica ristretta, come la clozapina.
È importante ricordare che queste interazioni farmacocinetiche sono causate dagli IPA, non dalla nicotina. La terapia sostitutiva con nicotina non contribuisce a queste interazioni.
Al contrario, le interazioni farmacodinamiche con il fumo di tabacco sono in gran parte dovute alla nicotina, poiché questa attiva il sistema nervoso simpatico e può contrastare le azioni farmacologiche di alcuni farmaci.
La caffeina è metabolizzata dal CYP1A2 quasi al 100% ed è spesso utilizzata negli studi come marcatore dell'attività di questo isoenzima. La sua clearance aumenta del 56% nei fumatori.
Quando un paziente smette di fumare, l'assunzione di caffeina andrebbe dimezzata per evitare livelli di caffeina eccessivi.
I sintomi della tossicità da caffeina (irritabilità, insonnia) possono imitare quelli dell'astinenza da nicotina e generare confusione. È importante la valutazione dell'assunzione giornaliera totale di caffeina, da tutte le fonti di caffeina, anche bevande e integratori alimentari.
Analogamente, la teofillina, un’altra metilxantina, ha una clearance raddoppiata nei fumatori; dopo che un paziente smette di fumare l’emivita della teofillina può aumentare del 38%.
Molti dei farmaci con interazioni farmacocinetiche clinicamente significative sono utilizzati in psichiatria.
La clozapina (Leponex°), un antipsicotico atipico, è metabolizzato principalmente dal CYP1A2. Uno studio ha rilevato che a parità di posologia, i livelli medi di clozapina nel plasma dei fumatori erano circa l'80% di quelli dei non fumatori. Nei fumatori maschi l’effetto era amplificato, con una concentrazione di clozapina plasmatica solo del 68% rispetto alle concentrazioni dei non fumatori.
In uno studio sul metabolismo dell'olanzapina (Zyprexa°), altro antipsicotico atipico, nei fumatori sono state trovate concentrazioni plasmatiche allo steady state di 5 volte inferiori rispetto ai non fumatori. Nei fumatori la clearance dell'olanzapina può aumentare del 98%.
Anche le concentrazioni di fluvoxamina (Fevarin°), un antidepressivo SSRI, nei fumatori sono risultate significativamente inferiori (di circa un terzo) rispetto ai non fumatori.
Per quanto riguarda gli antidepressivi triciclici (amitriptilina, nortriptilina, clomipramina), non sembra siano necessari aggiustamenti posologici.
L'R-isomero (meno attivo) del warfarin è metabolizzato dall’isoenzima CYP1A2. Nei pazienti in terapia anticoagulante si può osservare un aumento dell’INR dopo la cessazione del fumo.
Farmaci per i quali è documentata un’interazione farmacocinetica con il fumo sono anche clorpromazina, aloperidolo, flecainide, propranololo, clopidogrel e altri (v. tabella al fondo).
Per quanto riguarda le interazioni farmacodinamiche, quella con il maggior significato clinico è con i contraccettivi estroprogestinici.
Il rischio cardiovascolare degli estroprogestinici è nettamente aumentato nelle fumatrici. Se queste desiderano una contraccezione farmacologica e i tentativi di cessazione del fumo non hanno successo, sono consigliabili contraccettivi a base di solo progesterone.
Per esempio, nelle donne che utilizzano un cerotto contraccettivo contenente etinilestradiolo e norelgestromina (Evra°) si è osservato che nelle fumatrici i livelli di estrogeni plasmatici sono più alti del 60% rispetto ai livelli ottenuti con un contraccettivo orale con 35 mcg di estrogeni.
Va notato che l'efficacia clinica dei contraccettivi ormonali non è ridotta nelle fumatrici.
Anche l’efficacia degli steroidi inalatori è ridotta negli asmatici che fumano, sempre con un meccanismo farmacodinamico. I fumatori possono quindi richiedere dosi più alte di steroidi inalatori per il controllo dell'asma.
💊 Altri post in tema
Interazioni farmacologiche e fumo
Focus Farmacovigilanza 2013;78(9):1
Smoking and drug interactions
Aust Prescr 2013;36:102-4
Drug interactions with smoking
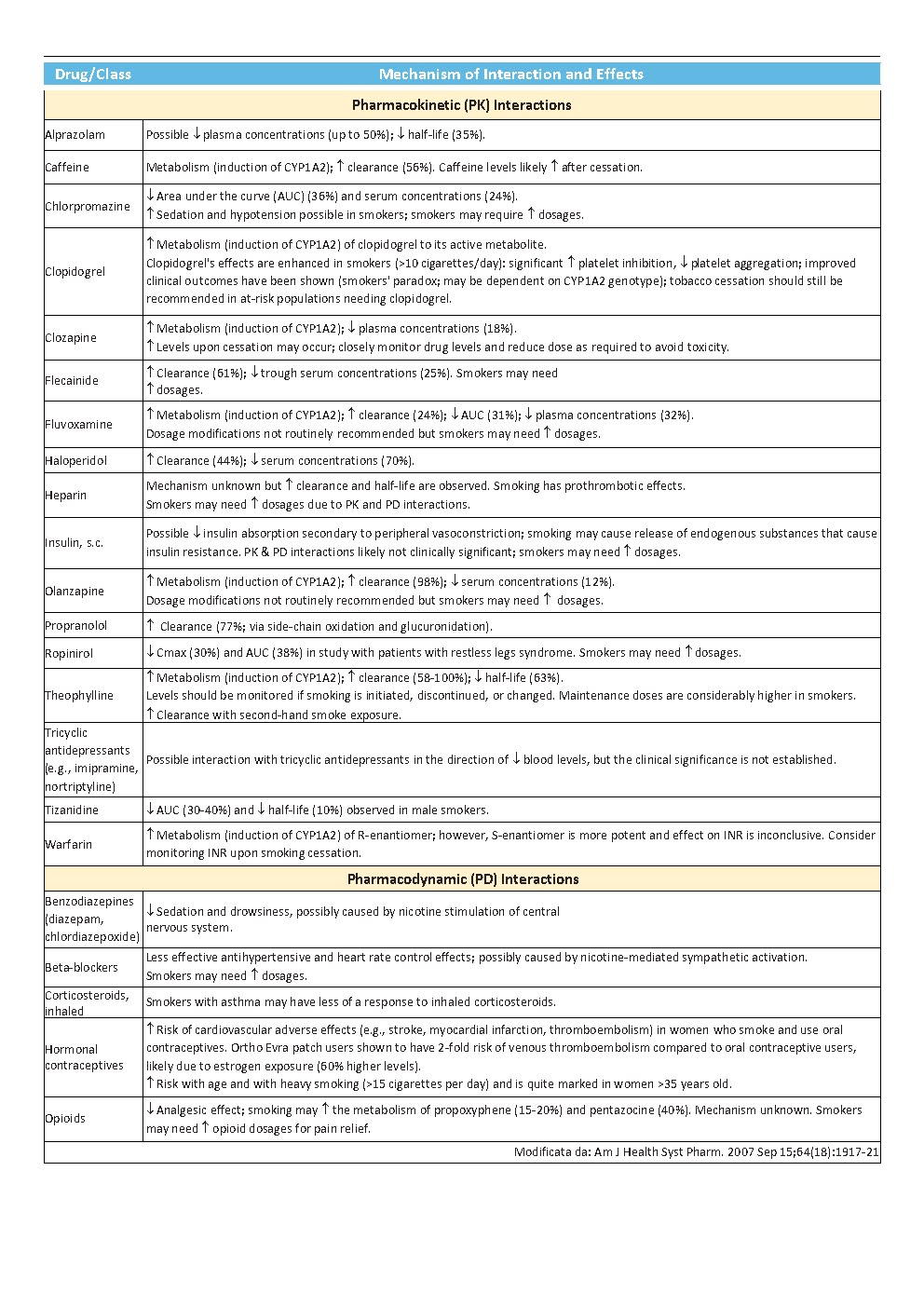
Am J Health Syst Pharm. 2007 Sep 15;64(18):1917-21
Drug Interactions Flockhart Table
Un utile schema su substrati e inibitori dei diversi isoenzimi del citocromo P450
Gilberto Lacchia - Pubblicato 30/04/2021 - Aggiornato 30/04/2021


Commenti
Posta un commento