È il farmaco che causa più frequentemente effetti avversi polmonari. La tossicità polmonare è frequente e grave, soprattutto se non riconosciuta come dipendente dalla terapia. [Lettura 7 min]
L’amiodarone è un antiaritmico indicato per la terapia e la prevenzione di aritmie gravi resistenti ad altre terapie specifiche. Viene di solito riservato a situazioni in cui altre terapie non possono essere utilizzate o sono fallite.
L'amiodarone è associato a numerosi effetti avversi:È un farmaco altamente lipofilo, che si concentra in molti tessuti e viene eliminato molto lentamente; l’emivita è di circa 50 giorni, e gli effetti avversi possono persistere per oltre un mese dopo la sospensione della terapia.
In alcune casistiche l’amiodarone è risultato il farmaco che più frequentemente causa tossicità polmonare (seguito dalla nitrofurantoina), che è anche uno dei suoi effetti avversi più gravi.
La scheda tecnica dell’amiodarone informa che la tossicità polmonare correlata all’assunzione di amiodarone è una reazione avversa “frequente e grave, che si può manifestare fin al 10% dei pazienti e che può essere fatale nell’8% dei soggetti colpiti, soprattutto a causa di una mancata diagnosi.”
Su Vigiaccess le segnalazioni di interstitial lung disease, pulmonary fibrosis, lung disorder, pulmonary toxicity, pneumonitis e lung infiltration rappresentano l’11% di tutte le segnalazioni.
Nei pazienti in terapia si possono verificare diverse forme di pneumopatia:
Patogenesi: sono state suggerite due ipotesi principali:
I sintomi si presentano in modo insidioso, con dispnea, tosse e calo ponderale in pazienti che assumono dosi ≥200 mg/d di amiodarone, in particolare da 6-12 mesi.
La febbre è presente nel 33-50% dei casi e possono essere segnalati anche altri sintomi, come dolore di tipo pleuritico o malessere generale.
L'esame obiettivo rivela spesso crepitii inspiratori bilaterali, mentre non è presente ippocratismo digitale.
Esami di laboratorio: sono aspecifici, con aumento dei globuli bianchi, della LDH, della proteina C reattiva e della VES. Di solito non sono presenti eosinofilia e anticorpi antinucleo.
I livelli di amiodarone sono di solito normali e non sono predittivi o diagnostici di tossicità polmonare.
Diagnostica per immagini: l'accumulo di amiodarone aumenta l'attenuazione dei tessuti a causa del contenuto di iodio. Si tratta di un marker di esposizione e si osserva nel fegato, nella milza e nel polmone atelettasico.
La radiografia del torace tipica nella polmonite interstiziale mostra nuove opacità diffuse o localizzate, reticolari, consolidative o miste.
La TC ad alta risoluzione (HRCT) può chiarire il pattern radiografico e la distribuzione delle anomalie.
L’amiodarone è un antiaritmico indicato per la terapia e la prevenzione di aritmie gravi resistenti ad altre terapie specifiche. Viene di solito riservato a situazioni in cui altre terapie non possono essere utilizzate o sono fallite.
L'amiodarone è associato a numerosi effetti avversi:
- cardiaci (bradicardia, arresto sinusale, prolungamento dell'intervallo QT, disturbi del ritmo ventricolare e rare torsades de pointes )
- tiroidei (ipotiroidismo, ipertiroidismo)
- oculari (depositi corneali, blefarospasmo, neurite ottica)
- gastroenterici (nausea, vomito, sapore metallico)
- neurologici (ipertensione intracranica, neuropatie periferiche, parestesie, atassia, tremori o altri sintomi extrapiramidali)
- cutanei (fotosensibilità, colorazione cutanea blu-grigia, sindrome di Stevens-Johnson, sindrome di Lyell)
- epatici (aumento delle transaminasi , epatiti, cirrosi)
- ematologici (anemia emolitica, aplasia midollare)
- polmonari (pneumopatie interstiziali, ecc.)
In alcune casistiche l’amiodarone è risultato il farmaco che più frequentemente causa tossicità polmonare (seguito dalla nitrofurantoina), che è anche uno dei suoi effetti avversi più gravi.
La scheda tecnica dell’amiodarone informa che la tossicità polmonare correlata all’assunzione di amiodarone è una reazione avversa “frequente e grave, che si può manifestare fin al 10% dei pazienti e che può essere fatale nell’8% dei soggetti colpiti, soprattutto a causa di una mancata diagnosi.”
Su Vigiaccess le segnalazioni di interstitial lung disease, pulmonary fibrosis, lung disorder, pulmonary toxicity, pneumonitis e lung infiltration rappresentano l’11% di tutte le segnalazioni.
Nei pazienti in terapia si possono verificare diverse forme di pneumopatia:
- polmonite interstiziale
- polmonite eosinofila
- sindrome da distress respiratorio acuto (ARDS)
- emorragia alveolare diffusa
- noduli polmonari e masse isolate
- versamenti pleurici (raramente)
Patogenesi: sono state suggerite due ipotesi principali:
- Citotossicità diretta sulle cellule polmonari: l'amiodarone ha un’elevata affinità tissutale per il polmone. Un metabolita attivo dell'amiodarone è citotossico e tende ad accumularsi nel tessuto polmonare ancor più dell'amiodarone stesso.
- Ipersensibilità: è suggerita dalle caratteristiche istopatologiche di una polmonite da ipersensibilità, con infiltrazione linfocitaria, linfocitosi e immunofluorescenza IgG positiva nel polmone.
- dose cumulativa (la tossicità polmonare si manifesta dopo mesi, di solito 6-12, o anni dall’inizio della terapia);
- posologia (l’incidenza è dell’1-5% con dosi giornaliere basse e del 5-15% con dosi >400 mg/d);
- durata della terapia >2 mesi;
- età e sesso (gli anziani di sesso maschile hanno maggior probabilità di essere colpiti);
- etnia (p.es. giapponesi)
- malattie polmonari preesistenti (è tuttavia possibile che questi pazienti abbiano una riserva polmonare limitata e sviluppino sintomi prima degli altri);
- ossigenoterapia ad alti flussi;
- interventi chirurgici e angiografia polmonare.
I sintomi si presentano in modo insidioso, con dispnea, tosse e calo ponderale in pazienti che assumono dosi ≥200 mg/d di amiodarone, in particolare da 6-12 mesi.
La febbre è presente nel 33-50% dei casi e possono essere segnalati anche altri sintomi, come dolore di tipo pleuritico o malessere generale.
L'esame obiettivo rivela spesso crepitii inspiratori bilaterali, mentre non è presente ippocratismo digitale.
Esami di laboratorio: sono aspecifici, con aumento dei globuli bianchi, della LDH, della proteina C reattiva e della VES. Di solito non sono presenti eosinofilia e anticorpi antinucleo.
I livelli di amiodarone sono di solito normali e non sono predittivi o diagnostici di tossicità polmonare.
Diagnostica per immagini: l'accumulo di amiodarone aumenta l'attenuazione dei tessuti a causa del contenuto di iodio. Si tratta di un marker di esposizione e si osserva nel fegato, nella milza e nel polmone atelettasico.
La radiografia del torace tipica nella polmonite interstiziale mostra nuove opacità diffuse o localizzate, reticolari, consolidative o miste.
La TC ad alta risoluzione (HRCT) può chiarire il pattern radiografico e la distribuzione delle anomalie.
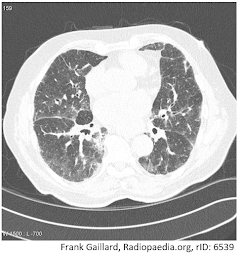
Si osservano opacità diffuse (di solito bilaterali) a vetro smerigliato e ispessimento dei setti, immagini a nido d’ape e bronchiectasie da trazione.
Ai test di funzionalità polmonare la pneumopatia da amiodarone è spesso associata a un quadro restrittivo.
In ambito specialistico possono essere eseguiti un lavaggio broncoalveolare e una biopsia polmonare in casi dubbi.
Trattamento: consiste principalmente nell'interruzione dell'amiodarone e, nei pazienti più sintomatici, steroidi sistemici (p.es. prednisone 40-60 mg/d).
A causa della lunga emivita, inizialmente la tossicità polmonare può progredire nonostante la sospensione del farmaco.
Ottenuta una risposta clinica, la terapia steroidea viene ridotta lentamente in 2-6 mesi. Se i sintomi e i segni si ripresentano, la dose di steroide viene di nuovo aumentata all’ultima dose efficace e l'ulteriore riduzione è più lenta, in circa 12 mesi.
I pazienti con sintomi lievi e ossigenazione normale possono essere osservati sospendendo l’amiodarone, senza somministrare cortisonici.
L’amiodarone non va più prescritto ai pazienti che hanno avuto una tossicità polmonare.
Screening: in alcune linee guida sono consigliate radiografie del torace periodiche per i pazienti in terapia con amiodarone. Questa pratica rischia di esporre eccessivamente alle radiazioni e di solito non è necessaria: il peggioramento della funzione respiratoria riferito dai pazienti è generalmente un buon indicatore precoce di tossicità polmonare.
È quindi importante che i pazienti conoscano i sintomi di tossicità polmonare, il fatto che può essere grave e che può verificarsi in qualsiasi momento durante la terapia, fino al mese successivo alla sospensione.
Prognosi: la prognosi della polmonite interstiziale da amiodarone è di solito favorevole se riconosciuta tempestivamente. In uno studio, per esempio, il 75% dei pazienti si sono stabilizzati o sono migliorati dopo la sospensione del farmaco con o senza terapia steroidea.
Ai test di funzionalità polmonare la pneumopatia da amiodarone è spesso associata a un quadro restrittivo.
In ambito specialistico possono essere eseguiti un lavaggio broncoalveolare e una biopsia polmonare in casi dubbi.
Trattamento: consiste principalmente nell'interruzione dell'amiodarone e, nei pazienti più sintomatici, steroidi sistemici (p.es. prednisone 40-60 mg/d).
A causa della lunga emivita, inizialmente la tossicità polmonare può progredire nonostante la sospensione del farmaco.
Ottenuta una risposta clinica, la terapia steroidea viene ridotta lentamente in 2-6 mesi. Se i sintomi e i segni si ripresentano, la dose di steroide viene di nuovo aumentata all’ultima dose efficace e l'ulteriore riduzione è più lenta, in circa 12 mesi.
I pazienti con sintomi lievi e ossigenazione normale possono essere osservati sospendendo l’amiodarone, senza somministrare cortisonici.
L’amiodarone non va più prescritto ai pazienti che hanno avuto una tossicità polmonare.
Screening: in alcune linee guida sono consigliate radiografie del torace periodiche per i pazienti in terapia con amiodarone. Questa pratica rischia di esporre eccessivamente alle radiazioni e di solito non è necessaria: il peggioramento della funzione respiratoria riferito dai pazienti è generalmente un buon indicatore precoce di tossicità polmonare.
È quindi importante che i pazienti conoscano i sintomi di tossicità polmonare, il fatto che può essere grave e che può verificarsi in qualsiasi momento durante la terapia, fino al mese successivo alla sospensione.
Prognosi: la prognosi della polmonite interstiziale da amiodarone è di solito favorevole se riconosciuta tempestivamente. In uno studio, per esempio, il 75% dei pazienti si sono stabilizzati o sono migliorati dopo la sospensione del farmaco con o senza terapia steroidea.
Drug-Induced Interstitial Lung Disease: A Systematic Review.
J Clin Med. 2018 Oct 15;7(10):356
Amiodarone pulmonary toxicity
UpToDate - topic last updated: Nov 30, 2021
Amiodarone lung
Radiopaedia - Last revised by on 12 Sep 2023
Gilberto Lacchia - Pubblicato 15/11/2023 - Aggiornato 15/11/2023



Commenti
Posta un commento